Epilepsie behandelen door de genetische fout bij een kind te corrigeren. Volgens Ype Elgersma is dat dé oplossing. “Over een paar jaar willen we deze therapie in de kliniek hebben.”
“Waar we onderzoek naar doen is: wat voor mutatie heeft een kind en kunnen we met RNA-therapie het effect van het genetische foutje ongedaan maken? Ik vind dat een spannende ontwikkeling.” Ype Elgersma is hoogleraar Moleculaire Neurobiologie in het Erasmus MC. Speciaal voor de ontwikkeling van deze veelbelovende behandeling stapte hij over van de afdeling Neurowetenschappen naar de afdeling Klinische Genetica. “Want ik denk dat daar de toekomst zit. Pak aan waar het probleem zit: in het DNA.”
Pleister plakken op genetische foutjes
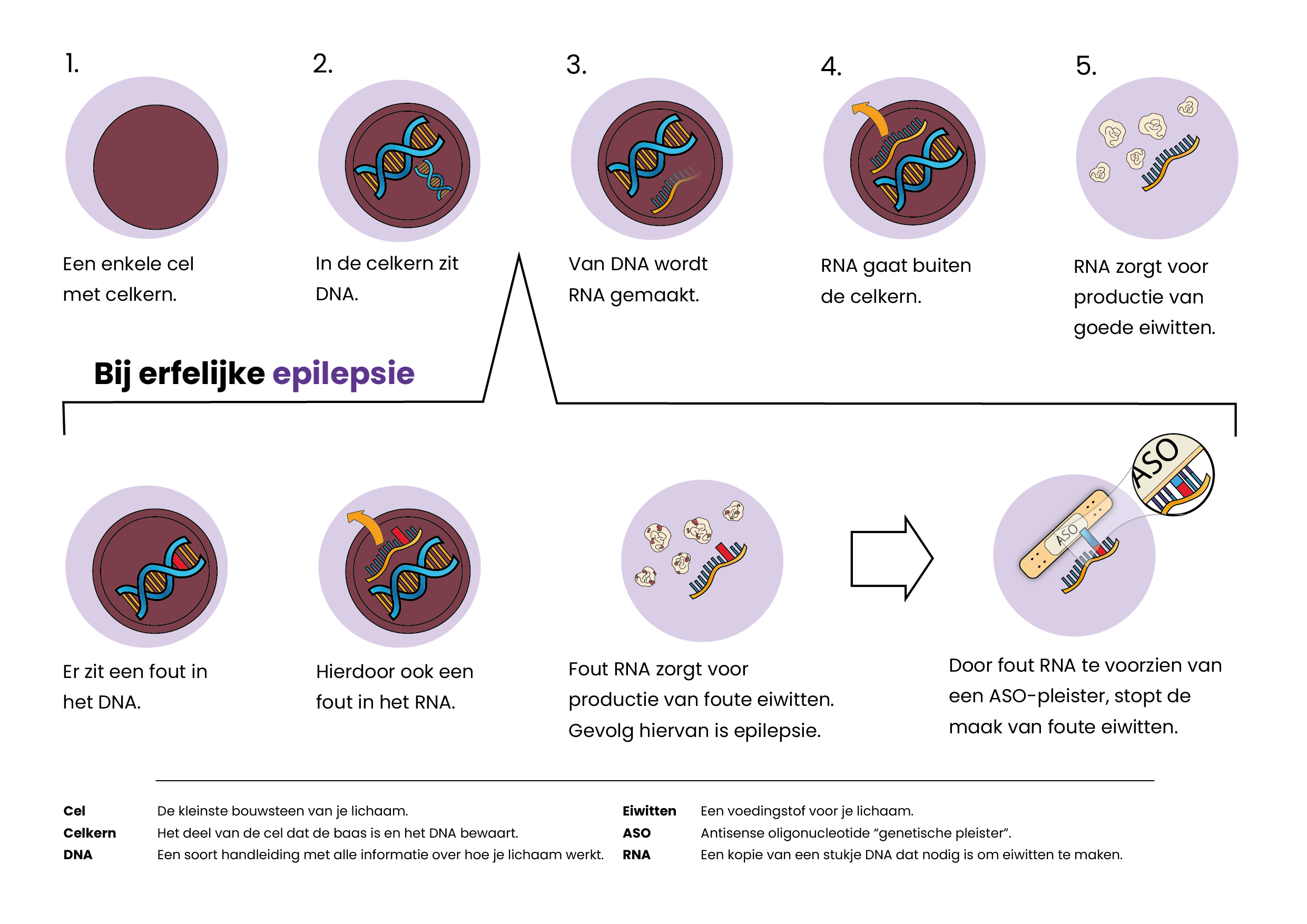
Het onderzoek dat Ype doet richt zich op kinderen. “Bij meer dan 30 procent van de kinderen met epilepsie is een mutatie in het DNA de onderliggende oorzaak.” Als je dit genetische foutje opspoort, kun je het repareren met RNA-therapie. Je plakt een soort genetische pleister op de fout. Daardoor werken de hersencellen weer zoals zou moeten en haal je de oorzaak van de epilepsie weg. “In muizen zien we volledige genezing. Maar de therapie werkt beter als je kinderen jong behandelt, omdat de hersenen dan nog in ontwikkeling zijn. En je wilt zo vroeg mogelijk beginnen met het brein beschermen tegen epileptische aanvallen. Want die zijn niet goed voor de ontwikkeling van een kind.”
Als voorbeeld voor de doorbraak van RNA-therapie noemt Ype de spierziekte SMA. Bij die aandoening sterven motorische zenuwcellen af en dat leidt tot verlamming. Ieder kind wordt op SMA gescreend met de hielprik. Met RNA-therapie kan deze levensbedreigende aandoening goed behandeld worden.
De behandeling werkt direct op de goede plek
Hoe wordt deze methode toegepast bij iemand met epilepsie? “Je neemt wat bloed af bij de patiënt. In het laboratorium kweek je stamcellen uit dit bloed op tot hersencellen. Je ontwikkelt een ‘genetische pleister’ en die test je op de gekweekte hersencellen. Als je ziet dat die cellen zich normaal gaan gedragen, dan kun je de ‘pleister’ aan de patiënt toedienen.” Dat gaat met een ruggenprik. De ingespoten stof (de ‘pleister’) bereikt via het hersenvocht de hersenen. “De hersencellen nemen deze ‘pleisters’ goed op, dus het werkt direct op de goede plek en hiermee pak je de oorzaak gericht aan.”
Dat is nog een voordeel voor de patiënt. Want ‘reguliere’ medicijnen tegen epilepsie hebben als nadeel dat ze ook andere hersenfuncties beïnvloeden. Iemand beweegt daardoor bijvoorbeeld moeilijker of wordt traag in zijn denken. Bij RNA-therapie gebeurt dat niet. “Je grijpt gericht in op het proces dat misgaat en niet op andere hersenprocessen.” De behandeling met een ruggenprik zou je drie keer per jaar moeten doen, verwacht Ype. Liefst zou hij willen dat het op het hoofd wordt toegediend. “Via een klein buisje (‘poort’) onder de huid dat daar blijft zitten.” Maar eerst moet de werking van de pleister bevestigd worden.
Unieke genetische pleister
“Voor één meisje zijn we al heel ver.” In de komende twee jaar verwacht Ype de unieke genetische pleister die hij voor haar ontwikkelt, te kunnen toepassen. “Dit is echt een op maat gemaakt medicijn.” Maar als in de toekomst iemand met dezelfde mutatie wordt gediagnosticeerd, kan dezelfde pleister worden gebruikt. “Voor alle foutjes die epilepsie veroorzaken en die zich ervoor lenen, wil ik een pleister ontwikkelen. Dat kost tijd, want je moet de pleisters testen. Maar we hopen het steeds sneller en goedkoper te kunnen doen door de processen te verbeteren.”
Open afbeelding“Onze droom is om na de genetische diagnose van de epilepsie, binnen een jaar de therapie aan een kind te kunnen toedienen.” Over een aantal jaren wil Ype zover zijn. “Het hele lab wordt daar nu op ingericht, want er is verschillende vakkennis én teamwerk voor nodig. Daar gaan we met ons allen voor.”